尽管 Aduhelm 是一种靶向淀粉样蛋白 β (Aβ) 的单克隆抗体,基于其降低 AD 患者 Aβ 斑块负担的能力,最近成为美国 FDA 批准的首个治疗阿尔茨海默病 (AD) 的药物,但其对认知改善的作用仍存在争议。此外,大约 40% 接受这种抗体治疗的患者出现严重的副作用,包括脑水肿 (ARIA-E) 和出血 (ARIA-H),这些副作用可能与 Aβ 抗体结合 Fc 受体 (FCR) 时大脑中的炎症反应有关) 免疫细胞,如小胶质细胞和巨噬细胞。这些炎症副作用可导致神经元细胞死亡和激活的小胶质细胞消除突触,甚至有可能加剧 AD 患者的认知障碍。因此,
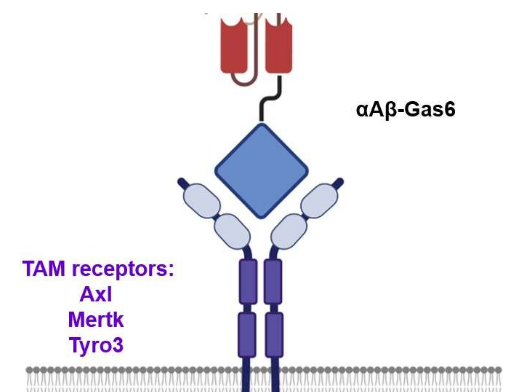
为了克服这些问题,韩国 KAIST 的一组研究人员开发了一种新型融合蛋白药物 αAβ-Gas6,它通过与基于 Aβ 抗体的免疫疗法完全不同的机制有效消除 Aβ。在 AD 小鼠模型中,αAβ-Gas6 不仅以更高的效力去除了 Aβ,而且还规避了与常规抗体治疗相关的神经毒性炎症副作用。
产生的 αAβ-Gas6 可清除 Aβ 寡聚体和原纤维,而不会引起神经毒性(ab,神经元:红色,和碎片轴突:黄色)和促炎反应(c,TNF 释放),相反,通过 Aβ 靶向单克隆抗体的治疗会加剧这些反应(阿杜卡单抗)。图片来源:Gliabiology Lab & Kim Lab of Immunotherapy
“因此,我们利用了胞吐作用,这是一种细胞过程,通过吞噬细胞去除死细胞作为清除大脑中 Aβ 的替代途径,”Kim 和 Chung 教授说。“胞吐作用伴随着抗炎反应以维持组织稳态。为了利用这一过程,我们设计了 Gas6,这是一种可溶性衔接蛋白,通过 TAM 吞噬受体介导胞吐作用,其靶特异性从死细胞重定向到 Aβ 斑块。”
教授和他们的团队证明,由此产生的 αAβ-Gas6 通过激活小胶质细胞和星形胶质细胞的吞噬作用来诱导 Aβ 吞噬,因为 TAM 吞噬受体在大脑中的这两个主要吞噬细胞中高度表达。重要的是,αAβ-Gas6 促进了 Aβ 的强烈摄取,而没有显示任何炎症和神经毒性迹象,这与使用 Aβ 单克隆抗体的治疗形成鲜明对比。此外,他们发现 αAβ-Gas6 显着减少了小胶质细胞对突触的过度消除,从而导致 AD 模型小鼠的行为得到更好的拯救。